Kalor didefinisikan sebagai energi panas yang dimiliki oleh suatu zat. Secara umum untuk mendeteksi adanya kalor yang dimiliki oleh suatu benda yaitu dengan mengukur suhu benda tersebut. Jika suhunya tinggi maka kalor yang dikandung oleh benda sangat besar, begitu juga sebaliknya jika suhunya rendah maka kalor yang dikandung sedikit.
Dari hasil percobaan yang sering dilakukan besar kecilnya kalor yang dibutuhkan suatu benda(zat) bergantung pada 3 faktor
- massa zat
- jenis zat (kalor jenis)
- perubahan suhu
Sehingga secara matematis dapat dirumuskan :
Q = m.c.(t2 – t1)
Dimana :
Q adalah kalor yang dibutuhkan (J)
m adalah massa benda (kg)
c adalah kalor jenis (J/kgC)
(t2-t1) adalah perubahan suhu (C)
Kalor dapat dibagi menjadi 2 jenis
- Kalor yang digunakan untuk menaikkan suhu
- Kalor yang digunakan untuk mengubah wujud (kalor laten), persamaan yang digunakan dalam kalor laten ada dua macam Q = m.U dan Q = m.L. Dengan U adalah kalor uap (J/kg) dan L adalah kalor lebur (J/kg)
Dalam pembahasan kalor ada dua kosep yang hampir sama tetapi berbeda yaitu kapasitas kalor (H) dan kalor jenis (c)
Kapasitas kalor adalah banyaknya kalor yang diperlukan untuk menaikkan suhu benda sebesar 1 derajat celcius.
H = Q/(t2-t1)
Kalor jenis adalah banyaknya kalor yang dibutuhkan untuk menaikkan suhu 1 kg zat sebesar 1 derajat celcius. Alat yang digunakan untuk menentukan besar kalor jenis adalah kalorimeter.
c = Q/m.(t2-t1)
Bila kedua persamaan tersebut dihubungkan maka terbentuk persamaan baru
H = m.c
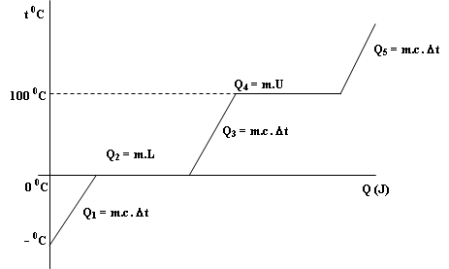
Analisis grafik perubahan wujud pada es yang dipanaskan sampai menjadi uap. Dalam grafik ini dapat dilihat semua persamaan kalor digunakan.
Keterangan :
Pada Q1 es mendapat kalor dan digunakan menaikkan suhu es, setelah suhu sampai pada 0 C kalor yang diterima digunakan untuk melebur (Q2), setelah semua menjadi air barulah terjadi kenaikan suhu air (Q3), setelah suhunya mencapai suhu 100 C maka kalor yang diterima digunakan untuk berubah wujud menjadi uap (Q4), kemudian setelah berubah menjadi uap semua maka akan kembali terjadi kenaikan suhu kembali (Q5)
Untuk mencoba kemampuan silakan kkerjakan latihan soal dengan cara klik disini.
Hubungan antara kalor dengan energi listrik
Kalor merupakan bentuk energi maka dapat berubah dari satu bentuk kebentuk yang lain. Berdasarkan Hukum Kekekalan Energi maka energi listrik dapat berubah menjadi energi kalor dan juga sebaliknya energi kalor dapat berubah menjadi energi listrik. Dalam pembahasan ini hanya akan diulas tentang hubungan energi listrik dengan energi kalor. Alat yang digunakan mengubah energi listrik menjadi energi kalor adalah ketel listrik, pemanas listrik, dll.
Besarnya energi listrik yang diubah atau diserap sama dengan besar kalor yang dihasilkan. Sehingga secara matematis dapat dirumuskan.
W = Q
Untuk menghitung energi listrik digunakan persamaan sebagai berikut :
W = P.t
Keterangan :
W adalah energi listrik (J)
P adalah daya listrik (W)
t adalah waktu yang diperlukan (s)
Bila rumus kalor yang digunakan adalah Q = m.c.(t2 – t1) maka diperoleh persamaan ;
P.t = m.c.(t2 – t1)
Yang perlu diperhatikan adalah rumus Q disini dapat berubah-ubah sesuai dengan soal.
Asas Black
Menurut asas Black apabila ada dua benda yang suhunya berbeda kemudian disatukan atau dicampur maka akan terjadi aliran kalor dari benda yang bersuhu tinggi menuju benda yang bersuhu rendah. Aliran ini akan berhenti sampai terjadi keseimbangan termal (suhu kedua benda sama). Secara matematis dapat dirumuskan :
Q lepas = Q terima
Yang melepas kalor adalah benda yang suhunya tinggi dan yang menerima kalor adalah benda yang bersuhu rendah. Bila persamaan tersebut dijabarkan maka akan diperoleh :
Q lepas = Q terima
m1.c1.(t1 – ta) = m2.c2.(ta-t2)
Catatan yang harus selalu diingat jika menggunakan asasa Black adalah pada benda yang bersuhu tinggi digunakan (t1 – ta) dan untuk benda yang bersuhu rendah digunakan (ta-t2). Dan rumus kalor yang digunakan tidak selalu yang ada diatas bergantung pada soal yang dikerjakan.
dikutip dari